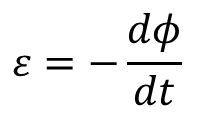¿Qué Es El Error De Faraday Por Factores Abióticos? La Guía Definitiva Para Científicos Y Técnicos
¿Alguna vez has obtenido lecturas electroquímicas que simplemente no encajan, a pesar de tener un protocolo impecable y equipos calibrados? La respuesta podría estar escondida en un concepto crítico y a menudo pasado por alto: el error de Faraday por factores abióticos. Este fenómeno es el "fantasma" que acecha en tus experimentos de voltametría, coulometría y cualquier técnica que dependa de la ley de Faraday, introduciendo inexactitudes sistemáticas que pueden invalidar resultados y desperdiciar recursos. Si trabajas en química analítica, ciencia de materiales, biología electroquímica o ingeniería ambiental, comprender y mitigar este error no es solo una buena práctica, es fundamental para la integridad de tu datos.
Este artículo desentrañará por completo el error de Faraday por factores abióticos. Exploraremos la física detrás de la ley de Faraday, definiremos con precisión qué constituye un "factor abiótico" en este contexto, analizaremos cómo y por qué estos factores distorsionan la relación carga-masa, y proporcionaremos un marco práctico para diagnosticar, cuantificar y corregir estos errores en el laboratorio. Desde la conductividad de la solución hasta la geometría del electrodo, dejaremos piedra sobre piedra para que puedas construir experimentos más robustos y publicables.
Comprendiendo los Cimientos: La Ley de Faraday y su Suposición Ideal
La Promesa de la Ley de Faraday
En su corazón, la ley de Faraday es una de las relaciones más bellas y útiles de la electroquímica. Establece que la cantidad de sustancia producida o consumida en un electrodo durante una reacción electroquímica es directamente proporcional a la cantidad de electricidad (carga, Q) que pasa a través de la celda. La fórmula es sencilla: m = (Q * M) / (n * F), donde m es la masa, M el peso molar, n el número de electrones transferidos y F la constante de Faraday (96,485 C/mol). Esta ley es el pilar de técnicas cuantitativas como la coulometría (donde se mide la carga para determinar la cantidad de analito) y la gravimetría electroquímica (donde se pesa el depósito formado).
El supuesto implícito y crítico es que el 100% de la carga que fluye a través del circuito externo se utiliza para impulsar la reacción redox deseada en el electrodo de trabajo. Cualquier desviación de este ideal—cualquier carga que se "pierde" en procesos parásitos—introduce un error de Faraday. Este error se manifiesta como una discrepancia entre la masa de producto esperada (calculada por la carga) y la masa real obtenida, o viceversa.
El Mundo Real vs. El Modelo Ideal: ¿Dónde se Escapa la Carga?
En un sistema electroquímico ideal, solo ocurre la reacción de interés. Sin embargo, en la práctica, la corriente total (I_total) que mide tu potenciostato o galvanostato se compone de múltiples componentes:I_total = I_reacción_deseada + I_reacciones_parásitas + I_otros_procesos
Las reacciones parásitas son el culpable más común del error de Faraday. Incluyen:
- Evolución de gases: La reducción de protones a hidrógeno (H₂) o la oxidación de agua a oxígeno (O₂) en potenciales donde también ocurre tu reacción objetivo.
- Reducción/oxidación de impurezas: Especies contaminantes en la solución o en los electrodos que se oxidan o reducen en el mismo rango de potencial.
- Corrientes de capacitancia (carga/descarga de la doble capa eléctrica): Un proceso no faradaico donde los iones se reorganizan en la interfaz electrodo-solución. Aunque es transitorio, en técnicas de barrido rápido puede contribuir significativamente a la carga total integrada.
Pero aquí es donde entra el concepto de factores abióticos. No son reacciones químicas en sí mismas, sino condiciones físicas y ambientales del sistema que alteran la eficiencia de la transferencia de electrones o la cuantificación de la carga, sesgando la aplicación de la ley de Faraday.
Desglosando el "Factor Abiótico": Más Allá de la Química
En el contexto del error de Faraday, un factor abiótico es cualquier componente o condición no viva (no biótica) del sistema experimental que afecta la relación lineal y estequiométrica entre la carga eléctrica aplicada/medida y la cantidad de producto químico formado. No son reactivos que se consumen, sino variables físicas y geométricas que distorsionan la medición.
Los Principales Factores Abióticos que Generan Error
Resistencia de la Solución (Rs): También llamada resistencia óhmica o caída de IR. Es la oposición al flujo de corriente a través de la solución electrolítica. Un valor alto de Rs provoca que el potencial que realmente se aplica en la interfaz electrodo-solución (
E_aplicada - I*Rs) sea menor que el potencial que configuras en el potenciostato. Esto puede hacer que tu reacción deseada no ocurra a la velocidad esperada (o en absoluto) en el potencial programado, forzando que parte de la corriente se desvíe a otras reacciones (parásitas) que sí son posibles a ese potencial efectivo más bajo. Es el factor abiótico más ubicuo y problemático.Geometría y Área del Electrodo: La ley de Faraday asume que la reacción ocurre de manera uniforme sobre el área electroactiva real. En la práctica:
- El área geométrica (lo que mides con un calibre) rara vez es igual al área electroactiva real (la superficie microscópicamente rugosa y activa).
- La distribución de corriente rara vez es uniforme. En electrodos grandes o de geometría compleja, la densidad de corriente es mayor en los bordes (efecto de borde), llevando a que la reacción se concentre en zonas específicas, dejando otras partes del electrodo "inactivas" o favoreciendo reacciones parásitas locales.
- Esto significa que para una carga Q dada, la masa depositada m será menor de lo esperado si el área real es menor que la asumida, introduciendo un error sistemático negativo.
Difusión Limitada y Convección: La ley de Faraday supone que los reactivos están disponibles en la interfaz en todo momento. En sistemas no agitados o con electrodos de disco, el transporte de especie activa desde la solución bulk hacia el electrodo por difusión puede ser más lento que la velocidad a la que la reacción quiere consumirla. Esto crea un "gradiente de concentración" y limita la corriente (corriente de difusión limitada). Si forzas una corriente mayor (en galvanostato) o aplicas un potencial más negativo (en potenciostato), la reacción deseada se detiene y la corriente "sobrante" se va inevitablemente a reacciones parásitas (como la evolución de H₂). La convección (agitación, burbujeo, movimiento natural) puede mitigar o exacerbar este problema de manera impredecible.
Temperatura: Aunque a menudo se controla, la temperatura afecta múltiples parámetros:
- Conductividad de la solución: Aumenta con la temperatura, reduciendo Rs.
- Viscosidad: Disminuye con la temperatura, mejorando los coeficientes de difusión.
- Constantes de equilibrio y cinética: Las velocidades de las reacciones parásitas y la deseada cambian con T, a menudo de manera diferente. Un cambio de temperatura no controlado altera la selectividad del sistema.
Composición y Propiedades del Electrolito: Más allá de la simple conductividad:
- Fuerza iónica: Afecta los coeficientes de actividad y, por ende, los potenciales de electrodo.
- Especies específicas: Iones que pueden adsorberse en el electrodo, bloqueando sitios activos (ej. cloruros en platino) o participando en complejos que alteran la cinética.
- pH: Es un factor abiótico crítico para reacciones que involucran protones o iones hidróxido. Un pH local en la interfaz puede ser drásticamente diferente al pH bulk debido a la generación/consumo de H⁺ u OH⁻, desviando la selectividad.
El Vínculo Crítico: Cómo los Factores Abióticos Distorsionan la Relación Carga-Masa
Volvamos a la ecuación de Faraday. El error surge porque, en la práctica, la carga efectiva utilizada para la reacción deseada (Q_efectiva) es menor que la carga total medida (Q_medida). El error porcentual se puede estimar como:
Error (%) ≈ [(Q_medida - Q_efectiva) / Q_efectiva] * 100
Los factores abióticos son los principales responsables de que Q_efectiva < Q_medida. Por ejemplo:
- Alta Rs: Para alcanzar el potencial deseado en el electrodo, necesitas aplicar un potencial externo más alto. Si ese potencial extra cae en la solución, no contribuye a la fuerza impulsora de la reacción deseada. La corriente que fluye a ese potencial "inflado" puede ser parcialmente consumida por la evolución de H₂ (una reacción parásita de bajo sobrepotencial), especialmente en cátodo.
Q_medidaincluye esta corriente parásita, peroQ_efectiva(para tu reacción) es menor. - Área Subestimada: Si tu electrodo tiene un área real 1.5 veces mayor que el área geométrica que usaste en tus cálculos, esperarías depositar 1.5 veces más masa para una carga dada. En realidad, depositas la masa correcta para el área real, pero como usaste un área más pequeña en la fórmula, tu masa calculada
m_calcserá 1.5 veces mayor que la masa realm_real. ¡Parece un error de exceso de producto, pero en realidad es un error de subestimación del área! - Difusión Limitada: Si la concentración de tu especie electroactiva en la interfaz cae a cero, la corriente de la reacción deseada se estabiliza en un máximo (corriente de difusión limitada). Cualquier intento de forzar más corriente (aumentando el potencial en potenciostato) resultará en que el exceso de corriente vaya directamente a la evolución de H₂. La carga total integrada (
Q_medida) será alta, pero solo una fracción (Q_efectiva) se usó para la reacción deseada.
Ejemplos Prácticos y Cómo se Manifiesta el Error
Ejemplo 1: Determinación de Cobre por Coulombimetría de Deposición
- Escenario: Depositas cobre(II) a un cátodo de platino desde una solución ácida (0.5 M H₂SO₄) con 10 mM Cu²⁺. Aplicas una corriente constante de 10 mA durante 1000 segundos (carga total = 10 C). Según Faraday, deberías depositar
m = (10 C * 63.55 g/mol) / (2 * 96485 C/mol) ≈ 0.033 gde Cu. - Realidad: Debido a la alta Rs (solución diluida en ácido) y el bajo sobrepotencial para H₂ en Pt, una parte significativa de la corriente (digamos 2 mA) se va a la evolución de hidrógeno. La corriente efectiva para Cu es solo 8 mA. La masa real depositada será
≈ 0.026 g. Tu cálculo basado en la carga total te dará un valor 27% más alto. Error por factor abiótico (Rs y selectividad).
Ejemplo 2: Estudio de Óxidos Metálicos por Voltametría Cíclica
- Escenario: Barres un electrodo de tungsteno en una solución de buffer para formar y reducir un óxido superficial. Integras la carga bajo el pico de reducción para estimar la cantidad de óxido.
- Realidad: El electrodo tiene una rugosidad superficial significativa (área real > área geométrica). La carga integrada es correcta para el área real. Si calculas el grosor del óxido usando el área geométrica, lo subestimarás drásticamente. Además, la adsorción competitiva de aniones del buffer (ej. fosfato) puede bloquear sitios, haciendo que la carga sea menor de lo esperado para una cobertura completa. Error por factor abiótico (área real y adsorción).
Ejemplo 3: Biosensores de Glucosa en Muestras Complejas
- Escenario: Mides glucosa en suero usando un electrodo de glucosa oxidasa. La enzima cataliza la oxidación de glucosa, consumiendo O₂ y produciendo H₂O₂, que se oxida en el electrodo.
- Realidad: El pH del suero varía, y la actividad de la enzima y el potencial de oxidación del H₂O₂ son sensibles al pH. La fuerza iónica y proteínas del suero pueden causar pérdida de enzima por adsorción no específica (un factor abiótico de la matriz) o alterar la difusión de glucosa y O₂. La carga medida no reflejará solo la glucosa, sino una combinación de estos efectos. Error por factor abiótico (matriz de muestra, pH, fuerza iónica).
Estrategias de Diagnóstico y Soluciones: Cómo Vencer el Error
Paso 1: Diagnóstico Sistemático
- Realiza un Experimento de "Blanco" o "Control": Ejecuta tu protocolo completo en una solución sin el analito de interés (ej. sin Cu²⁺, sin glucosa). Cualquier carga medida aquí se debe enteramente a procesos parásitos y factores abióticos (evolución de gases, doble capa, oxidación de impurezas del electrolito). Resta esta carga de fondo de tus medidas con analito.
- Varía la Velocidad de Barrido (en Voltametría): Si el pico de tu reacción escala linealmente con la raíz cuadrada de la velocidad de barrido (
v^1/2), es difusión limitada. Si escala linealmente conv, es un proceso adsortivo/capacitivo dominante. Un mal escalamiento indica que la cinética o el transporte no son ideales. - Mide y Compensa la Resistencia (Rs): Usa la función de compensación de resistencia de tu potenciostato. Mide Rs independientemente (ej. con electroimpedancia espectroscópía, EIS, en el régimen de alta frecuencia) y ajústala. Observa cómo cambia la forma de tus ondas voltamétricas. Una compensación adecuada suele agudizar los picos y reducir la corriente en potenciales donde ocurren reacciones parásitas.
- Caracteriza el Área Real del Electrodo: Para electrodos metálicos, usa el método de la carga de la doble capa en un electrolito no reaccionante (ej. KCl 0.1 M) o técnicas como la microscopía de fuerza atómica (AFM). Para electrodos de pasta de carbono o modificados, métodos como la voltametría de redox de ferro/ferricianuro (asumiendo un coeficiente de transferencia estándar) son comunes. ¡Nunca asumas que el área geométrica es el área real!
- Controla la Temperatura y la Agitación: Usa un baño termostático. En técnicas estáticas, considera el uso de un rotor (ej. disco de rotación de electrodo, RDE) para establecer un flujo laminar controlado y eliminar la convección natural errática. La velocidad de rotación se convierte en un parámetro controlable que define el espesor de la capa de difusión.
Paso 2: Estrategias de Mitigación en el Diseño Experimental
- Selección del Electrolito de Soporte: Usa un electrolito de alta pureza y alta fuerza iónica (ej. KCl, KNO₃, Na₂SO₄) para minimizar Rs y estabilizar el potencial de unión líquida. Evita aniones que puedan adsorberse o complejarse (ej. Cl⁻ puede formar complejos con metales pesados o adsorberse en Au, Pt).
- Optimización del Potencial/Corriente: No trabajes en potenciales extremos donde las reacciones parásitas (evolución de gases) sean inevitables. Usa barridos lentos para minimizar corrientes capacitivas. En coulometría, usa potenciales controlados por tiempo (chronoamperometría) en lugar de corrientes controladas si la selectividad es un problema.
- Diseño de la Celda: Minimiza la distancia entre electrodos de trabajo y contraelectrodo para reducir Rs. Usa un puente salino o una unión líquida porosa para aislar el electrodo de referencia de contaminación. Asegura una buena agitación o flujo controlado si la difusión es limitante.
- Calibración con Patrones: Este es el antídoto final. Nunca confíes ciegamente en la ley de Faraday para cuantificación absoluta. Siempre realiza una curva de calibración usando estándares de concentración conocida en una matriz lo más parecida posible a tu muestra. La calibración empírica absorbe todos los errores sistemáticos (factores abióticos, eficiencia de deposición, área real) en una sola constante de respuesta. Es la práctica más robusta.
Preguntas Frecuentes (FAQ) sobre el Error de Faraday por Factores Abióticos
Q1: ¿El error de Faraday es lo mismo que la eficiencia de corriente?
R: Están íntimamente relacionados. La eficiencia de corriente (η) para una reacción se define como η = (carga utilizada para la reacción deseada) / (carga total suministrada). Un error de Faraday ocurre cuando asumes η=100% (ley de Faraday ideal) pero en realidad η<100% debido a factores abióticos y bióticos. Medir η experimentalmente (por ejemplo, pesando el depósito y calculando la carga que debería haberlo producido) es una forma de cuantificar este error.
Q2: ¿Los factores abióticos son más importantes que los bióticos (como enzimas o microbios)?
R: En un contexto puramente electroquímico sintético, los factores abióticos son los únicos culpables. Sin embargo, en bioelectroquímica (biosensores, microbios electrógenos), los factores bióticos (actividad enzimática, viabilidad microbiana, metabolismo) se suman a los abióticos. El error total es la combinación. Para un biosensor, un cambio de pH (abiótico) puede inactivar la enzima (biótico), multiplicando el error.
Q3: ¿Puedo ignorar el error si mis experimentos son solo cualitativos (ej. identificar un pico)?
R: Para identificación pura (potencial de pico), los factores abióticos pueden desplazar el potencial (por Rs, pH) pero a menudo no lo eliminan. Sin embargo, si intentas comparar intensidades de pico entre experimentos (ej. "el pico es más grande, por lo que hay más analito"), estás cuantificando y el error es crítico. La forma del pico también se distorsiona por Rs y difusión.
Q4: ¿La compensación de IR soluciona todos los problemas?
R: No. Es crucial para la selectividad de potencial (asegurar que el potencial en el electrodo sea el que crees), pero no corrige errores en la cuantificación de carga debidos a un área real mal estimada o a la adsorción competitiva. Es una herramienta necesaria pero no suficiente.
Q5: ¿Existe un "factor abiótico" universal que deba controlar siempre?
R: Sí. Los tres pilares son: 1) Caracterización precisa del área electroactiva real.2) Medición y compensación de la resistencia de la solución (Rs).3) Uso de un electrolito de soporte de alta pureza y fuerza iónica adecuada. Implementar estos tres elimina la mayor parte del error sistemático evitable.
El Futuro: Automatización, Modelado y Estándares
La comunidad científica está avanzando hacia la estandarización de reportes electroquímicos (iniciativas como las de la International Union of Pure and Applied Chemistry, IUPAC). Se recomienda encarecidamente reportar: el tipo de electrodo, el área geométrica y el método para estimar el área real, la resistencia de la solución medida, la temperatura, la velocidad de agitación (si aplica) y la composición exacta del electrolito.
El modelado computacional (simulaciones de dinámica de fluidos acopladas a transporte de masa y reacción) está permitiendo predecir cómo la geometría de la celda y el electrodo afectan los perfiles de concentración y potencial, ayudando a diseñar sistemas con mínima distorsión. Además, técnicas como la electroimpedancia espectroscópía (EIS) se están integrando en flujos de trabajo rutinarios no solo para medir Rs, sino para caracterizar la capacitancia de la doble capa (que correlaciona con área real) y los procesos de transferencia de carga, ofreciendo una "firma" completa del sistema que puede usarse para detectar desviaciones.
Conclusión: De la Física a la Práctica Rigurosa
El error de Faraday por factores abióticos no es una curiosidad teórica; es una fuente de error cuantitativo que socava la repetibilidad, la precisión y la credibilidad de innumerables experimentos electroquímicos. Su esencia radica en olvidar que la ley de Faraday describe un sistema idealizado, y que el mundo real está lleno de resistencia, geometrías imperfectas, limitaciones de transporte y propiedades físicas variables.
Dominar este concepto significa evolucionar de ser un simple operador de equipos a ser un arquitecto de sistemas electroquímicos. Requiere un cambio mental: de "¿qué potencial debo aplicar?" a "¿cómo está configurado mi sistema físico para que la carga que mido se convierta eficientemente en la reacción que deseo?". Implica adoptar el hábito de la caracterización completa del sistema (área, Rs, temperatura) y la calibración empírica con patrones como prácticas no negociables.
Al identificar, cuantificar y corregir activamente los factores abióticos—la resistencia de la solución, el área real del electrodo, los límites de difusión, la temperatura y la composición del electrolito—elevas tus datos de meras lecturas a mediciones confiables. No solo improves la exactitud de tus resultados, sino que construyes una base experimental tan sólida que resiste el escrutinio de revisores y colegas. En la búsqueda de la verdad química y material, entender y controlar el error de Faraday no es un lujo, es el estándar de oro de la ciencia electroquímica rigurosa.